Ντραγκάνα Νικίτοβιτς, Ph.D., ERT
Ντραγκάνα Νικίτοβιτς, Ph.D., ERTΑναπληρώτρια Καθηγήτρια
Ιστολογίας - Εμβρυολογίας
e-mail: nikitovic@uoc.gr
γραφείο: 2810 39 4557
εργαστήριο: 2810 39 4735
Ολοκληρωμένες και τρέχουσες ερευνητικές μελέτες του εργαστηρίου Ιστολογίας-Εμβρυολογίας
- Μελέτη της σύνθεσης και της κατανομής των GAGs σε MG-63 και Saos 2 κυτταρικές σειρές ανθρώπινου οστεοσαρκώματος, υψηλού και χαμηλού μεταστατικού δυναμικού αντίστοιχα. Τα αποτελέσματα της μελέτης έδειξαν ότι αμφότερες οι κυτταρικές σειρές συνθέτουν εξωκυττάριο υαλουρονικό οξύ (HA) καθώς και εκκρινόμενες και κυτταρικά προσκολλημένες γαλακτοζαμινογλυκάνες (GalAGs) και θειϊκή ηπαράνη (HS). Αν και αμφότερες οι κυτταρικές σειρές συνθέτουν αξιοσημείωτες ποσότητες PGs, τα Saos 2 κύτταρα παράγουν HA, GalAGs και HS σε σημαντικά χαμηλότερες ποσότητες από αυτές των MG-63 κυττάρων. Μελετήθηκε επίσης η δράση της genistein στη σύνθεση αυτών των μορίων. Η ανασταλτική επίδραση της genistein στη σύνθεση των εξωκυττάρια εκκρινόμενων και των κυτταρικά προσκολλημένων GAGs/PGs στα Saos 2 κύτταρα βρέθηκε να είναι δοσοεξαρτώμενη, και πιο πιθανόν μέσω ενός PTK μηχανισμού. Η σύνθεση των GAGs/PGs από τα MG-63 κύτταρα με την παρουσία της genistein εξαρτάται από το τύπο και την κατανομή τους, υποδηλώνοντας ένα πιο σύνθετο μηχανισμό που ρυθμίζει την σύνθεση των PGs.
- Εξέταση της δράσης των TGF-β2, bFGF και PDGF-BB στη σύνθεση και κατανομή των GAGs/PGs στις δύο κυτταρικές σειρές οστεοσαρκώματος. Τα αποτελέσματα έδειξαν ότι η δράση των αυξητικών παραγόντων διαφέρει μεταξύ των δύο κυτταρικών σειρών και ότι η ρύθμιση στη σύνθεση των GAGs εξαρτάται από τον τύπο και την κατανομή τους. Τροποποιήσεις της δομικής σύστασης των συστατικών των GAGs/PGs της εξωκυττάριας θεμέλιας ουσίας μπορεί να έχει σημαντικές συνέπειες στο πολλαπλασιασμό των κυττάρων ή / και τη διαφοροποίηση τους. Σε οστεοβλάστες ανθρώπου, καθώς και στις MG-63 και Saos 2 κυτταρικές σειρές οστεοσαρκώματος, χορηγήθηκαν στη συνέχεια οι κυριότεροι τύποι αλυσίδων GAGs π.χ. η θειϊκή χονδροϊτίνη (CSA), θειϊκή δερματάνη (DS) και η ηπαρίνη (Hep) και μελετήθηκε η επίδρασή τους στην ανάπτυξη αυτών των κυττάρων. Τα αποτελέσματά έδειξαν ότι οι GAGs της εξωκυττάριας θεμέλιας ουσίας είναι μακρομόρια που επηρεάζουν τη κυτταρική ανάπτυξη των κακοήθων και των φυσιολογικών κυττάρων οστεοβλαστικής αρχής με μια δοσοεξαρτώμενη συμπεριφορά. Αυτή η επίδραση σχετίζεται στενά με τη λεπτομερή χημική δομή των GAGs, όπως για π.χ. είναι η παρουσία L-ιδουρονικού οξέος και ο βαθμός της θείωσής τους. Επιπρόσθετα, λαμβάνοντας υπ’ όψην ότι ο TGF-β2, ο bFGF και ο PDGF-BB είναι σημαντικοί ρυθμιστές της έκφρασης των μακρομορίων της εξωκυττάριας θεμέλιας ουσίας, η επίδραση αυτών των αυξητικών παραγόντων στην έκφραση των διαφόρων ισομορφών της βερσικάνης, μια μεγάλου μεγέθους πρωτεογλυκάνης θειϊκής χονδροϊτίνης, στην σύνθεση της συνθάσης του ΗΑ από τα MG-63 κύτταρα του οστεοσαρκώματος αλλά και από φυσιολογικούς ανθρώπινους οστεοβλάστες του περιοδοντικού συνδέσμου (hPDL). Τα αποτελέσματα έδειξαν ότι ο TGF-β2 προκαλεί την έκφραση της βερσικάνης και του HA από τα κύτταρα του ανθρώπινου οστεοσαρκώματος ενώ ο PDGF-BB είχε την κύρια επίδραση του στην έκφραση της HAS2 ισομορφής και της βιοσύνθεσης του HA από τους οστεοβλάστες. Συμπερασματικά, ο TGF-β2 μπορεί να έχει ρόλο στη μεταστατική δυνατότητα των κυττάρων του ανθρώπινου οστεοσαρκώματος.
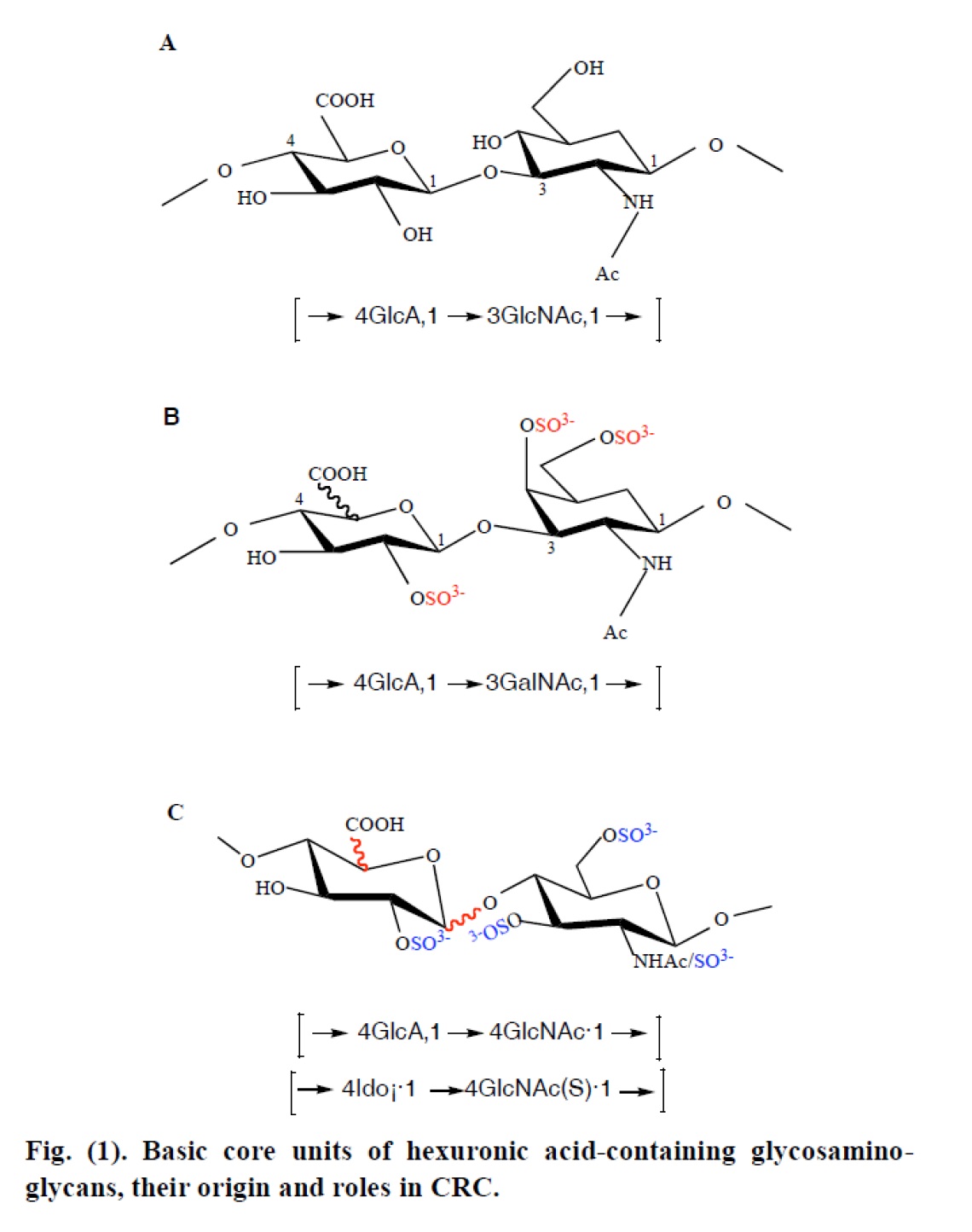
- Μελέτη του ρόλου των αλυσίδων θειϊκής χονδροϊτίνης Α (CSA) στον πολλαπλασιασμό, στην προσκόλληση, στη μετανάστευση, καθώς και στο χημειοτακτισμό, κυττάρων ινοσαρκώματος και φυσιολογικών ινοβλαστών. Με βάση τα αποτελέσματα της έρευνας, ρόλο-κλειδί για τη δράση της CSA διαδραματίζουν οι κινάσες τυροσίνης, αλλά και το ενδοκυτταρικό σηματοδοτικό μονοπάτι JNK (μέρος του MAPK μονοπατιού). Πιο συγκεκριμένα, σε κύτταρα του ινοσαρκώματος, η CSA ενισχύει τη δράση του αυξητικού παράγοντα των αιμοπεταλίων (PDGF), χρησιμοποιώντας μοριακή σηματοδότηση που συμπεριλαμβάνει κινάσες της τυροσίνης. Από την άλλη πλευρά, σε φυσιολογικούς ινοβλάστες, η CSA παρεμποδίζει την PDGF- επαγώμενη ενεργοποιήση του υποδοχέα β του αυξητικού παράγοντα των αιμοπεταλίων (PDGF-R beta), παρεμποδίζοντας τον πολλαπλασιασμό των κυττάρων. Συμπερασματικά, οι αλυσίδες θειϊκής χονδροϊτίνης αυξάνουν την κινητικότητα των κυττάρων του ινοσαρκώματος μέσω του MAPK σηματοδοτικού μονοπατιού. Εντούτοις, η CS-επαγώμενη μετανάστευση απαιτεί σηματοδοτικά μονοπάτια που εξαρτώνται από κινάσες της τυροσίνης.
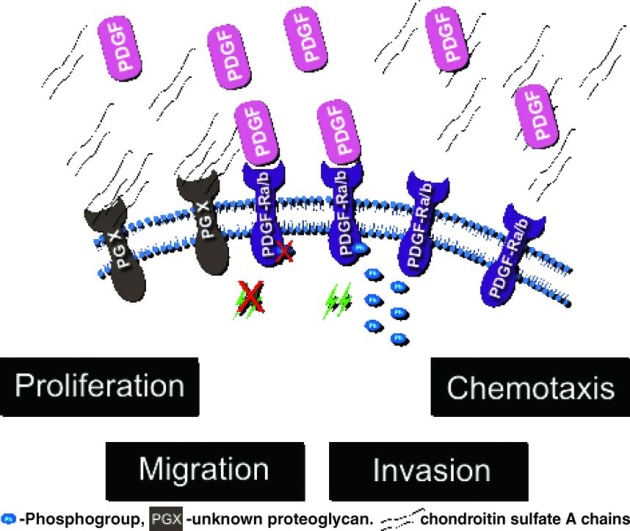
- Έρευνα του ρόλου των πρωτεογλυκανών και των γλυκοζαμινογλυκανών, στον πολλαπλασιασμό, στην προσκόλληση και στη μετανάστευση κυττάρων μελανώματος και φυσιολογικών μελανινοκυττάρων. Κατά τη διάρκεια της έρευνας διερευνήθηκε η δράση του FGF-2 στις βιολογικές ιδιότητες των κυττάρων, καθώς και η επίδραση του στα ενδοκυτταρικά σηματοδοτικά μόρια Erk1/2 και FAK. Επίσης, δείχθηκε ότι οι πρωτεογλυκάνες, που περιλαμβάνουν αλυσίδες θειϊκής χονδροϊτίνης και θεϊκής δερματάνης, σε συνεργασία με τις αλυσίδες θειϊκής ηπαράνης, συμμετέχουν στην πολλαπλασιαστική δράση που επάγει ο FGF-2. Τέλος, η λουμικάνη, μια μικρή-πλούσια σε λευκίνη πρωτεογλυκάνη (SLRP) εκφράζεται και εκκρίνεται από τα κύτταρα του μελανώματος, αλλά όχι και από τα φυσιολογικά μελανινοκύτταρα.
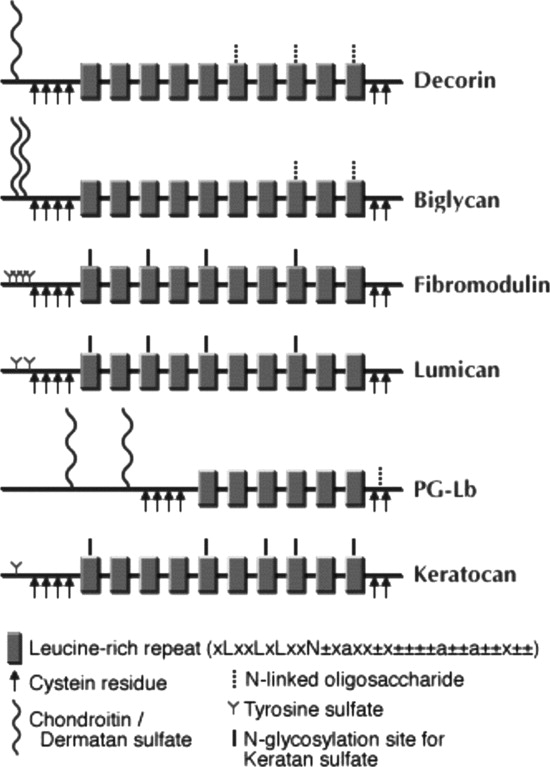
- Εξέταση του ρόλου των πρωτεογλυκανών και των γλυκοζαμινογλυκανών στις βιολογικές λειτουργίες καρκινικών κυττάρων του κόλον. Η παραγωγή των πρωτεογλυκανών και των γλυκοζαμινογλυκανών στα κύτταρα αυτά ρυθμίζεται, τόσο από τους υποδοχείς των οιστρογόνων, όσο και από σηματοδοτικά μονοπάτια κινασών της τυροσίνης. Η έρευνα αυτή εισηγήθηκε έναν νέο ρόλο για την ηπαρίνη, καθώς, σημαντικά γονίδια κρίσιμα για τη ρύθμιση του κυτταρικού κύκλου τροποποιούν την έκφραση τους, υπό την επίδραση της γλυκοζαμινογλυκάνης αυτής. Η δράση αυτή επιτυγχάνεται μέσω του σηματοδοτικού ενδοκυτταρικού διαμεσολαβητή p38 MAPK.
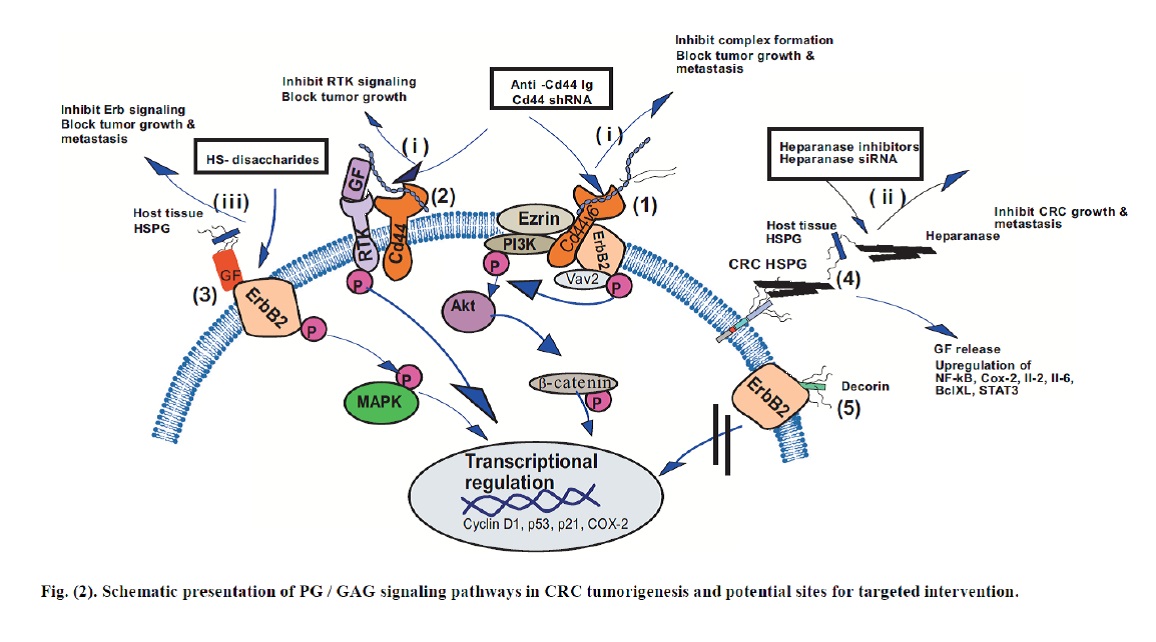
- Μελέτη του ρόλου της ηπαρίνης και των πρωτεογλυκανών θειϊκής ηπαράνης στις κυτταρικές λειτουργίες κυττάρων μελανώματος. Στη συγκεκριμένη μελέτη αποδείχθηκε ο ρόλος της ηπαρίνης υψηλού μοριακού βάρους στη ρύθμιση της προσκόλλησης και της μετανάστευσης, μέσω ενδοκυτταρικής σηματοδότησης που περιλαμβάνει τα p53 και FAK. Επιπλέον, δείχθηκε ότι ο FGF-2 τροποποιεί την προσκόλληση και τη μετανάστευση των κυττάρων του μελανώματος μέσω ενός μηχανισμού, εξαρτώμενου από τη συνδεκάνη-4. Επιπρόσθετα, η ηπαρίνη χαμηλού βάρους μέσω μείωσης της pPKCa και ανακατανομή της στην πυρηνική περιοχή, εμποδίζει την ενεργοποίηση της JNK. Τέλος, βρέθηκε ότι η JNK επάγει με τη σειρά της, αλλαγές στην οργάνωση του κυτταροσκελετού, που σχετίζονται με μειωμένη κυτταρική προσκόλληση.
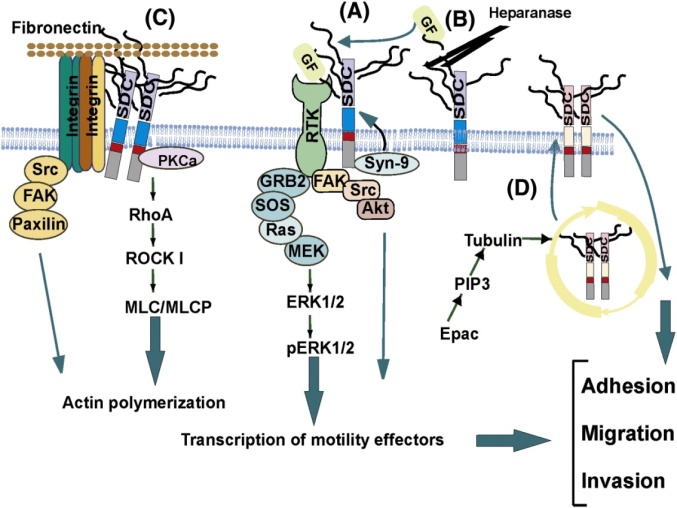
- Το οστεοσάρκωμα χαρακτηρίζεται από εναπόθεση άφθονης, μη ασβεστοποιημένης (mineralized) εξωκυττάριας ουσίας. Έτσι, εξετάστηκε ο τρόπος με τον οποίο αλλαγές στην εξωκυττάρια ουσία, επιδρούν στη μετανάστευση κυττάρων οστεοσαρκώματος. Πιο συγκεκριμένα, τα αποτελέσματα έδειξαν ότι οι αλλαγές στο μεταβολισμό του υαλουρονικού οξέος, που επάγονται από τη δράση πεπτιδίων της παραθορμόνης (PTH 1-34, PTH 7-84), σχετίζονται με αλλαγές στη μεταναστευτική ικανότητα των κυττάρων. Η μελέτη αυτή πραγματοποιήθηκε σε κύτταρα οστεοσαρκώματος MG-63 και Saos 2 (μέτρια διαφοροποιημένα και καλά διαφοροποιημένα κύτταρα οστεοσαρκώματος, αντίστοιχα). Η μελέτη αυτή προτείνει έναν ρυθμιστικό ρόλο για την PTH (1-34), στο μεταβολισμό του υαλουρονικού οξέος, που είναι σημαντικός για τη μετανάστευση των κυττάρων του οστεοσαρκώματος. Παράλληλα, η παραθορμόνη επηρεάζει την FGF- εξαρτώμενη σηματοδότηση, που ρυθμίζει τη μεταναστευτική ικανότητα των κυττάρων.
- Εξέταση του ρόλου του υαλουρονικού οξέος και των υποδοχέων του CD44 και RHAMM στη ρύθμιση των βιολογικών λειτουργιών κυττάρων του ινοσαρκώματος. Στην περίπτωση του ινοσαρκώματος απαντάται άφθονη εξωκυττάρια ουσία, με υψηλή περιεκτικότητα σε υαλουρονικό οξύ, πρωτεογλυκάνες, κολλαγόνο, ινονεκτίνη και λαμινίνη. Τα αποτελέσματα της μελέτης αυτής, προτείνουν έναν ρόλο κλειδί για την αλληλεπίδραση του υαλουρονικού οξέος και του RHAMM στη ρύθμιση της προσκόλλησης κυττάρων ινοσαρκώματος. Η δράση αυτή ενδοκυτταρικά, επιτυγχάνεται μέσω ενεργοποίησης των σηματοδοτικών μορίων FAK και Erk 1/2.
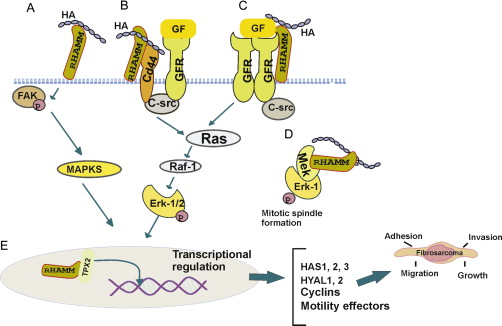
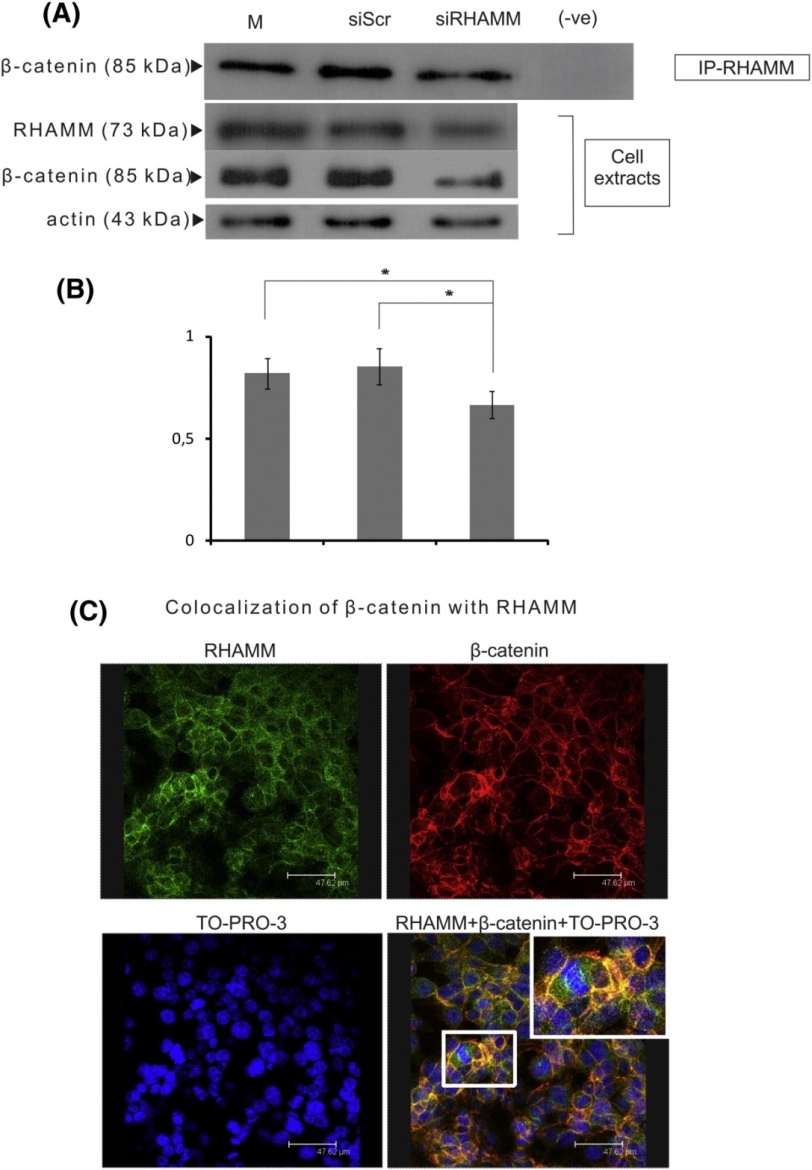
Επιπλέον, αποδείχθηκε ένας νέος ρόλος για το RHAMM, ο οποίος προσδένεται με τη β-κατενίνη, και προστατεύεται από την αποδόμηση. Η μετακίνηση του στον πυρήνα, έχει ως αποτέλεσμα, την ενεργοποίηση του c-myc, που ενισχύει την πολλαπλασιαστική ικανότητα των κυττάρων του ινοσαρκώματος. Στην τρέχουσα μελέτη εξετάζεται ο ρόλος του RHAMM στην σηματοδότηση της β-κατενίνης σε διαφορετικούς τύπους καρκίνων σε in vitro μοντέλα (ινοσάρκωμα, χονδροσάρκωμα, οστεοσάρκομα).
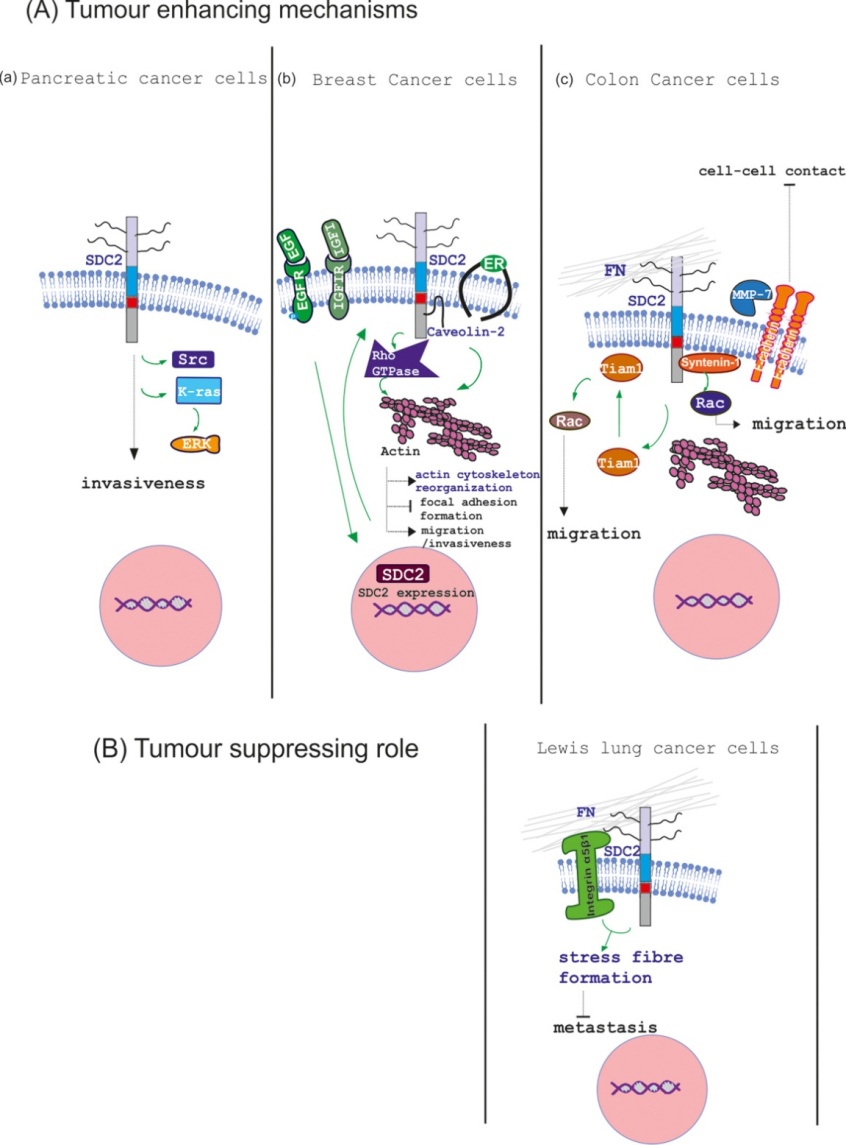
- Μελέτη της δυνατότητας του TGFβ2 να ενισχύει την προσκόλληση των κυττάρων ΗΤ1080 στην ινονεκτίνη (FN) μέσω ενός μηχανισμού όπου εμπλέκεται η συνδεκάνη 2 (SDC2) και το Smad2. Έχει αποδειχθεί ότι οι HS αλυσίδες επηρεάζουν την επαγόμενη από τον TGFβ προσκόλληση των ΗΤ1080 κυττάρων. Στην συγκεκριμένη μελέτη δείχνουμε για πρώτη φορά τη συνύπαρξη της SDC2 μαζί με τον IGF-IR, αναδεικνύοντας έτσι τη SDC2 ως πιθανό συν-υποδοχέα για τον ΙGF-I με τη κατάντι ενεργοποίηση του ΕRΚ1/2, η οποία είναι γνωστό ότι ρυθμίζει τη μεταγραφή απαραίτητων γονιδίων για τη συμπεριφορά του κυττάρου. Παράλληλα, επιβεβαιώσαμε ότι η ezrin συνυπάρχει με τη SDC2, καθώς και με την ακτίνη στις έντονες μικροπροσεκβολές των κυττάρων ΗΤ1080, ρυθμίζοντας εν μέρει καταυτόν τον τρόπο την κινητικότητα και την επιθετική συμπεριφορά των κυττάρων.
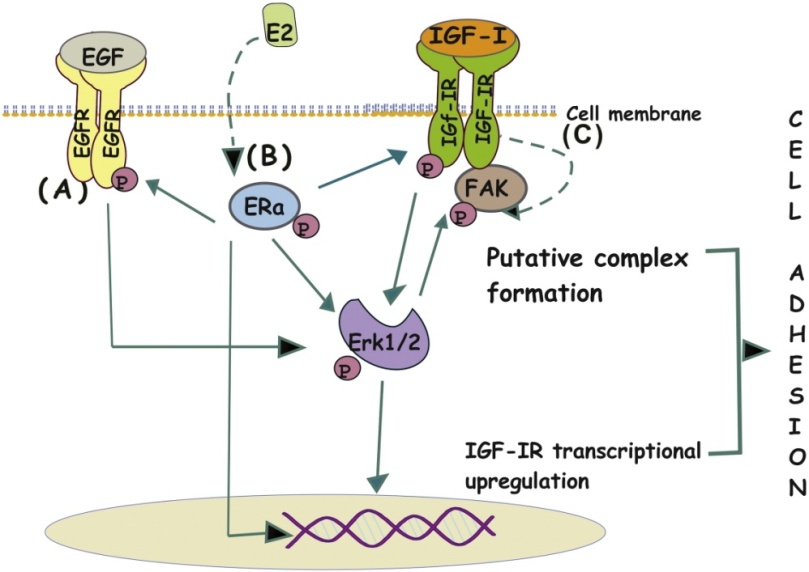
- Μελέτη του ρόλου των αυξητικών παραγόντων EGF και IGF και των υποδοχέων τους EGFR, HER-2 και IGFR, στη λειτουργία καρκινικών κυττάρων του μαστού και της συμβολής των μακρομορίων του εξωκυττάριου χώρου. Στην συγκεκριμένη μελέτη εξετάστηκαν οι αλληλεπιδράσεις των μοριακών σηματοδοτικών μονοπατιών των Ε2 και των IGF-I/EGF, στην προσκόλληση των καρκινικών κυττάρων του μαστού καθώς και οι πιθανοί ενδοκυτταρικοί διαμεσολαβητές. Η ινονεκτίνη, συστατικό που βρίσκεται σε αφθονία στην εξωκυττάρια θεμέλια ουσία των καρκινικών κυττάρων του μαστού, είναι μία μεγάλου μοριακού βάρους γλυκοπρωτεΐνη, που έχει χαρακτηριστεί δείκτης επιθετικότητας για τη βιοπαθολογία του καρκίνου του μαστού. Στην παρούσα μελέτη, έχει δειχθεί ότι τόσο οι IGF-I/EGF όσο και η Ε2 ενισχύουν σημαντικά την προσκόλληση των MCF-7 καρκινικών κυττάρων του μαστού σε υπόστρωμα ινονεκτίνης. Επιπλέον, ο βασικός υποδοχέας του IGF-I, ο IGF-IR, είναι απαραίτητος για την επαγωγή της προσκόλλησης από τους IGF-I/EGF και Ε2. Η αναστολή του Erk1/2 εμποδίζει την IGF-I- /EGF- /E2- εξαρτώμενη προσκόλληση των MCF-7 κυττάρων, καταδεικνύοντας ότι ο Erk1/2 είναι σημαντικός ενδοκυττάριος διαμεσολαβητής σήματος των παραγόντων αυτών για τη συγκεκριμένη κυτταρική λειτουργία. Η χορήγηση IGF-I και EGF επάγει την αναδιοργάνωση των ινιδίων ακτίνης του κυτταροσκελετού στα MCF-7 καρκινικά κύτταρα του μαστού. Η αναδιοργάνωση αυτή φαίνεται να τροποποιείται από την αναστολή του Erk1/2, που είναι ο βασικός κυτταρικός διαμεσολαβητής των IGF-I και EGF. Ενδιαφέρον παρουσιάζει το δεδομένο ότι η χορήγηση του IGF-I επάγει το συν-εντοπισμό των IGF-IR και FAK, που είναι ορατός κυρίως κοντά στις κυτταρικές μεμβράνες των MCF-7 κυττάρων. Τα δεδομένα αυτά καταδεικνύουν ότι ο IGF-IR είναι σημείο συνάντησης για την IGF-/ EGF- και Ε2- εξαρτώμενη κυτταρική προσκόλληση σε υπόστρωμα ινονεκτίνης.
- Μελέτη της δράσης των μικρών πλούσιων σε λευκίνη μικρών πρωτεογλυκανών (SLRP) στις βιολογικές λειτουργίες των όγκων μεσεγχυματικής αρχής εστιάζοντας στο οστεoσάρκωμα και χονδροσάρκωμα. Η μελέτη αυτή απέδειξε ότι η SLRP λουμικάνη εκφράζεται από τα κύτταρα του ανθρώπινου οστεοσαρκώματος με τρόπο εξαρτώμενο από τα στάδιο της διαφοροποίησης των κυττάρων αυτών. Η λουμικάνη επηρεάζει το πολλαπλασιασμό, τη μετανάστευση και τη χημειοτακτική απάντηση στην ινονεκτίνη των κύτταρων του ανθρώπινου οστεοσαρκώματος μερικώς μέσω του άξονα TGF-Β2/Smad2. Eκτός τούτου βρέθηκε ότι η όγκο-κατασταλτική SLRP, διακοσμιτίνη, δεν επάγει την έκφραση της p21WAF-1, ούτε προκαλεί παρατεταμένη αναίρεση και αδρανοποίηση του EGFR. Αντίθετα, ο EGFR φάνηκε να υπερεκφράζεται και να παραμένει δια μακρόν φωσφορυλιωμένος. Επιπρόσθετα, παρατηρήθηκε ότι για τα αυξημένα επίπεδα του EGFR δεν χρειάζεται ενεργοποιημένη σηματοδότηση του EGFR, υποδηλώνοντας ότι μπορεί να επιτευχθεί σταθεροποίηση των υποδοχέων αυτών μέσω των αλληλεπιδράσεων της εξωκυττάριας διακοσμιτίνης και του EGFR. Σαν συμπέρασμα συνάγεται ότι τα MG-63 κύτταρα είναι ανθεκτικά στην αναστολή της ανάπτυξης που προκαλείται από την διακοσμιτίνη.
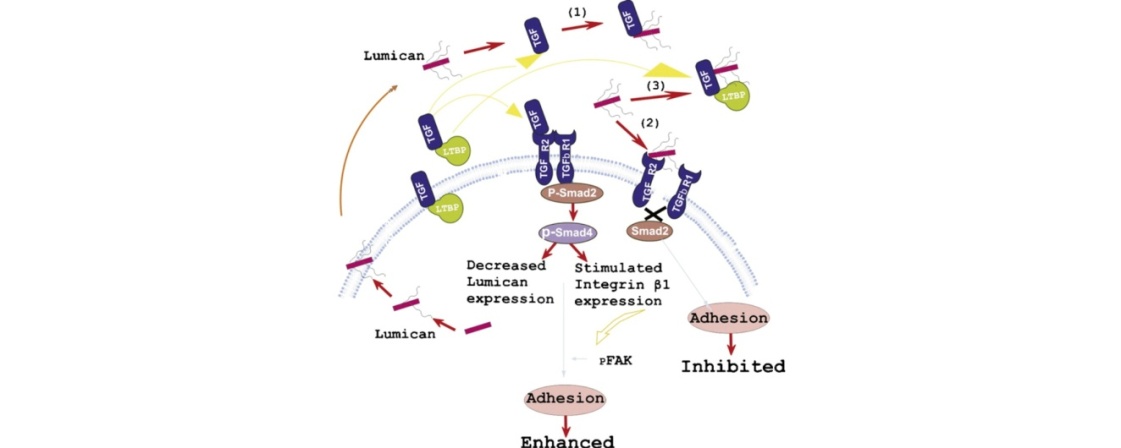
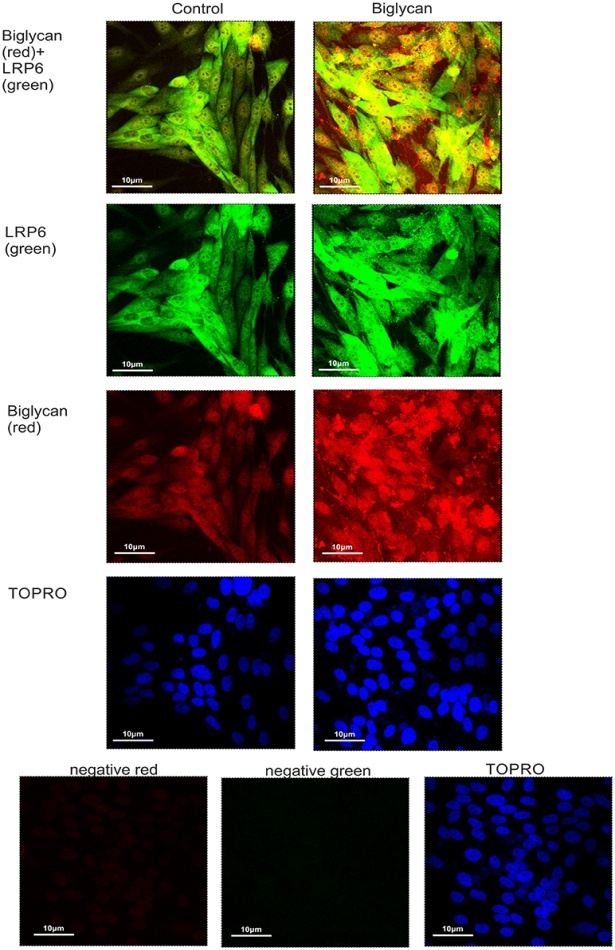
Βρήκαμε, επίσης ένα νέο μηχανισμό όπου η SLRP διγλυκάνη μέσω ενός άξονα σηματοδότησης LRP6 / β-κατενίνης / IGF-IR ενισχύει την ανάπτυξη κυττάρων του οστεοσαρκώματος. Συνεχίζεται η μελέτη του ακριβή μηχανισμού της δράσης της διγλυκάνης στα κύτταρα MG63. Επικεντρωνόμαστε στην ταυτοποίηση των συστατικών του συμπλέγματος ενδοκυττάριου συν-εντοπισμού IGF-IR / β-κατενίνης καθώς και σε συγκεκριμένους πιθανούς ρυθμιστές. Η σημασία αυτού του μηχανισμού θα ερευνηθεί και σε άλλες κυτταρικές σειρές οστεοσαρκώματος, όπως την Saos2, καθώς και σε άλλους όγκους μεσεγχυματικής προέλευσης, όπως τα κύτταρα χονδροσαρκώματος HTB94. Ταυτόχρονα, μελετάμε την δράση της διγλυκάνης και της λουμικάνης στις κυτταρικές λειτουργίες των κυττάρων του χονδροσαρκώματος σε συνδυασμό με τους αυξητικούς παράγοντες TGFβ2 και IGF-I. Έχει βρεθεί ότι τα HTB94 κύτταρα χονδροσαρκώματος εκφράζουν τη λουμικάνη που ρυθμίζει το πολλαπλασιασμό των κυττάρων αυτών μέσω ενός IGF-IR / Erk1,2 / p53 σημματοδοτικού άξονα.
- Μελέτη της δράσης του υαλουρονικού οξέως (ΗΑ) στην ενεργοποίηση των κερατινοκυττάρων από αλλεργιογόνα. Η επαφή του δέρματος με ανεπιθύμητους βιομηχανικούς ή περιβαλλοντικούς παράγοντες μπορεί να οδηγήσει στην εκδήλωση της δερματίτιδας εξ επαφής (ACD) είτε αλλεργικής είτε ερεθιστικής αιτιολογίας. Kατά την διάρκεια της φλεγμονής ή του τραυματισμού, απελευθερώνονται μόρια της ECM μεταξύ των οποίων τμήματα του μικρού μοριακού βάρους υαλουρονικού οξέος (HA) που δρουν ως μοριακά μοτίβα που σχετίζονται με βλάβες (damage- associated molecular patterns, DAMPs) ή «σήματα κινδύνου», δηλαδή ενδογενή μόρια που προκαλούν και ενισχύουν την φλεγμονή.
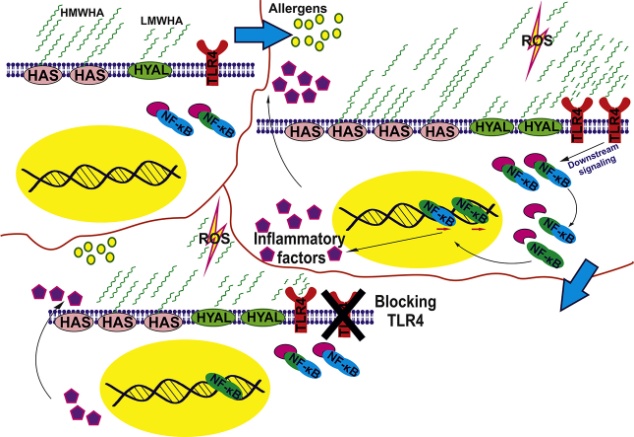
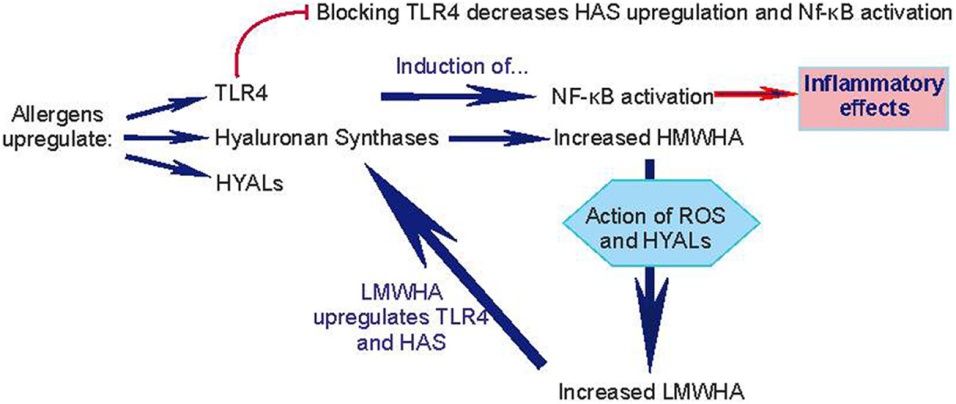
H oμάδα μας έδειξε ότι η αποικοδόμηση του ΗΑ στα κερατινοκύτταρα μεταβάλλεται μετά από επώαση με αλλεργιογόνα όπως το DNCB και PPD. Επιπλέον, βρέθηκε ότι το χαμηλού μοριακού βάρους υαλουρονικό (LWMHA) προκαλεί παραγωγή ιντερλευκίνης- 18, δείκτη της ενεργοποίησης των κερατινοκυττάρων. Βρήκαμε ότι τα αλλεργιογόνα PPD και DNCB προκάλεσαν σημαντική αύξηση του υποδοχέα TLR4 με τρόπο εξαρτώμενο από τη συγκέντρωσή τους, στην κυτταρική σειρά ανθρώπινων κερατινοκυττάρων NCTC2544. Συμπερασματικά, η ενεργοποίηση των κερατινοκυττάρων καθορίζεται μερικώς από τον σηματοδοτικό άξονα χαμηλού μοριακού βάρους υαλουρονικό οξύ/ TLR4/ NF-κB.
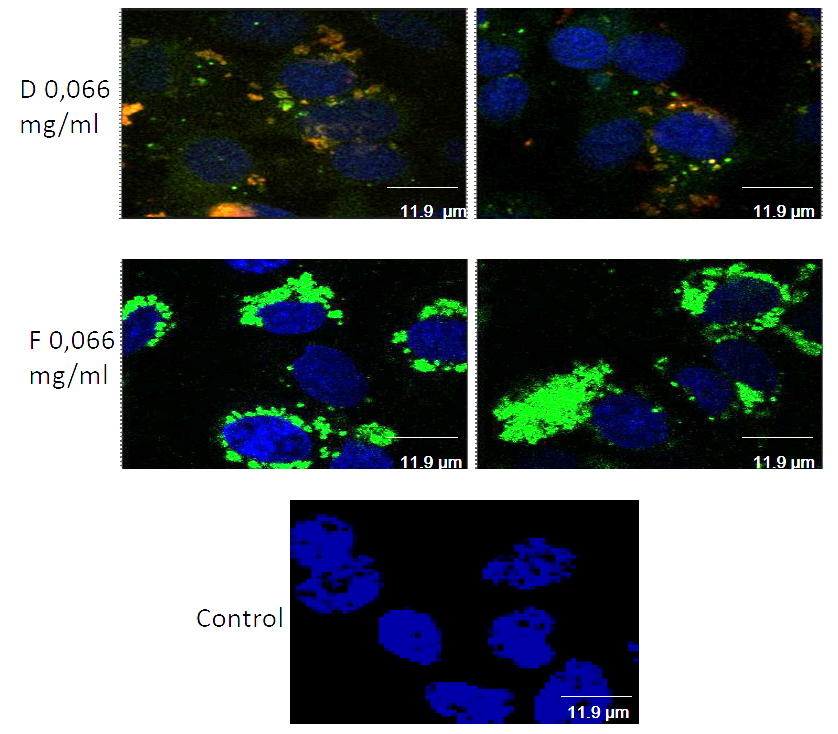
- Μελέτη των αλληλεπιδράσεων των νανοσωματιδίων και του αιματοεγκεφαλικού φραγμού: η αξιολόγηση της ανοσολογικής ενεργοποίησης και του ρόλου της υποενδοθηλιακής εξωκυττάριας θεμέλιας ουσίας. Ο αιματεγκεφαλικός φραγμός (ΒΒΒ), αποτελεί ένα λειτουργικό κυτταρικό φραγμό μεταξύ του ιστού και των ενδοθηλιακών κυττάρων. Σκοπός αυτής της μελέτης είναι η αξιολόγηση της πιθανής ανοσολογικής ενεργοποίησης των ενδοθηλιακών κυττάρων με χορήγηση μιας σειράς από νανοσωματίδια PVP(5) ξεχωριστά ή ως σύμπλοκα φορέα-φαρμάκου. Εξετάσθηκε η έκφραση βιοδεικτών ενδοθηλιακής δυσλειτουργίας και η συγγένεια σύνδεσης των λευκοκυττάρων του περιφερικού αίματος με το στρώμα ενδοθηλιακών κυττάρων. Καθώς η ECM ανασχηματίζεται έντονα στη φλεγμονή σχεδιάστηκε και πραγματοποιείται στο εργαστήριό μας η μελέτη πιθανών επιδράσεων των νανοσωματιδίων στην έκφραση υποενδοθηλιακών ECM συστατικών συμπεριλαμβανομένων του κολλαγόνου IV, της ινωδονεκτίνης, της λαμινίνης, της ηπαράνης και της θειικής χονδροϊτίνης.

INNOvation with GLYcans
Faculty of Medicine, University of Crete
Hybrid Symposium
27-29 September
Heraklion, Greece & Zoom Platform
Poster, Timetable


Special Issue
"Exploring the Multifaceted Roles of Glycosaminoglycans (GAGs) - New Advances and Further Challenges"
Editors
Dr. Dragana Nikitovic
Dr. Serge Perez
Website
Special Issue
"The Role of Extracellular Matrix in Cancer Development and Progression"
Editors
Professor George Tzanakakis
Professor Dragana Nikitovic
Website